Infertilidade sem causa aparente: tudo o que você precisa saber para manejar o paciente na sua prática clínica!
A infertilidade sem causa aparente (ISCA) continua a desafiar mesmo os profissionais mais experientes da medicina reprodutiva. A infertilidade sem causa aparente refere-se à ausência de uma causa definida para a incapacidade de um casal alcançar a gravidez após 12 meses de tentativas, apesar de uma avaliação detalhada, ou após seis meses em mulheres com 35 anos ou mais
Apesar de não haver uma causa identificável clara, a ISCA representa um dilema clínico significativo que requer uma abordagem cuidadosa.
Prováveis etiologias da infertilidade sem causa aparente
Várias hipóteses foram propostas para explicar por que alguns casais não conseguem conceber na ausência de uma causa identificável.
Dentre as principais:
- Mudanças sutis no desenvolvimento folicular, na ovulação e na fase lútea em algumas mulheres nessas circunstâncias
- Análises do sêmen dos parceiros masculinos revelam concentração e motilidade espermática no limite inferior da faixa normal
- Falhas na implantação
- Fatores cervicais sutis
- Problemas com transporte e interação de espermatozoides e óvulos.
Além disso, muitos casos de infertilidade inexplicada resultam da interação complexa de múltiplos fatores, como a idade avançada da mulher com diminuição da reserva ovariana e parâmetros normais, porém no limite inferior da normalidade, do sêmen do parceiro masculino. Cada um desses fatores, isoladamente, pode não reduzir significativamente a fertilidade, mas combinados podem diminuir a taxa de gravidez.
Como conduzir o diagnóstico de infertilidade feminina?
A investigação do potencial reprodutivo feminino pode ser concluída, na maioria das mulheres, em um único ciclo menstrual. Este método proporciona um dinamismo maior na avaliação clínica, resultando na redução da ansiedade e do estresse conjugal.
É importante que a paciente não esteja tomando medicamentos que possam causar alterações hormonais. Além disso, é importante manter a citopatologia do colo uterino sempre atualizada. Embora o exame físico e ginecológico possa fornecer informações valiosas, os testes complementares são essenciais para uma avaliação precisa.
Lista de exames para avaliação da fertilidade feminina de acordo com os dias do ciclo menstrual regular de 28 dias:
| Exame | 2° a 4° dia | 7° a 12° dia | 10° a 14° dia | 21° a 28° dia |
|---|---|---|---|---|
| Perfil hormonal | X | |||
| Hormônio antimülleriano | X | |||
| Sorologias completas | NE | NE | NE | NE |
| Tipagem sanguínea | NE | NE | NE | NE |
| Cariótipo | NE | NE | NE | NE |
| Histerossalpingografia | X | |||
| Histeroscopia | X | |||
| Ultrassom transvaginal | X | |||
| Pesquisa de trombofilias | NE | NE | NE | NE |
Perfil hormonal para mulheres com ciclos regulares
Inclui:
- FSH
- LH
- Estradiol
- Prolactina e TSH, realizados pela manhã com jejum de pelo menos quatro horas.
Perfil hormonal para mulheres com ciclos irregulares
Mulheres com ciclos irregulares frequentemente apresentam distúrbios hormonais subjacentes que podem impactar a fertilidade. A avaliação hormonal é geralmente realizada no início do ciclo menstrual, preferencialmente entre o terceiro e quinto dia do ciclo. Inclui:
- FSH
- LH
- Estradiol
- Prolactina
- TSH
- 17-hidroxiprogesterona
- Androstenediona
- Testosterona total
- Cortisol
- SDHEA
- DHEA
- Glicemia de jejum
- Insulina em jejum.
Esses exames devem ser realizados no início do ciclo, com jejum de oito horas, pela manhã.
Hormônio antimülleriano
Produzido pelas células da granulosa dos folículos ovarianos em desenvolvimento, o AMH fornece uma estimativa direta da reserva ovariana, ou seja, do número de óvulos ainda disponíveis nos ovários.
Apesar de variar pouco ao longo do ciclo menstrual, é preferível solicitá-lo durante a fase folicular inicial, sem o uso de contraceptivos hormonais ou tratamentos hormonais para doenças como endometriose e adenomiose.
Sorologias completas
Incluem hepatite B, hepatite C, HIV I/II, rubéola, toxoplasmose, citomegalovírus, sífilis, HTLV I/II e sarampo. A sorologia para Zika vírus IgM deve ser solicitada no início do tratamento reprodutivo, com validade de 30 dias.
Cariótipo
Pode-se solicitar de rotina ou diante de casos de abortamento recorrente, falhas repetidas de implantação embrionária, má resposta ao tratamento hormonal, suspeita de síndromes genéticas e falência ovariana prematura (neste caso, também solicitar pesquisa de X frágil por PCR).
Histerossalpingografia
É o melhor exame para avaliar a função tubária e a competência do trato reprodutivo feminino para alcançar uma gravidez natural ou após tratamento com IIU.
Não deve-se solicitar em casos de diagnóstico atual de hidrossalpinge, devido ao risco de abscesso tubo-ovariano por agudização de doença inflamatória pélvica.
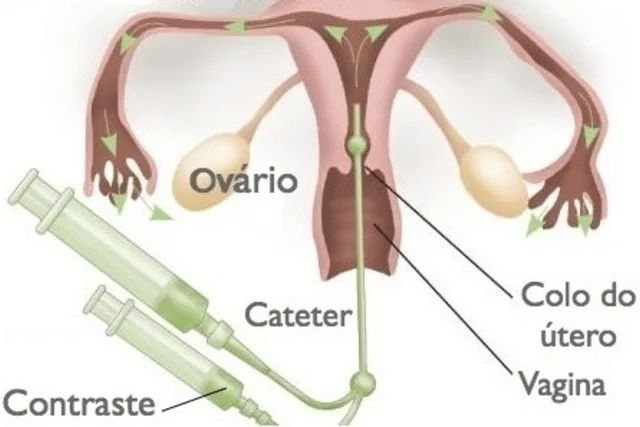
O procedimento começa com a inserção de um espéculo na vagina, seguido pela introdução de um cateter através do colo do útero. Injeta-se um contraste radiopaco na cavidade uterina, à medida que o contraste preenche a cavidade uterina e as trompas de Falópio, retira-se radiografias sequenciais. Essas imagens mostram o contorno da cavidade uterina e o trajeto do contraste pelas trompas, revelando possíveis obstruções ou anormalidades.
Histeroscopia diagnóstica
A histeroscopia diagnóstica é uma ferramenta essencial no arsenal de técnicas para avaliar a cavidade uterina em casos de infertilidade.
Este procedimento permite uma visualização direta do interior do útero, fornecendo informações detalhadas que não podem ser obtidas através de outros métodos de imagem, como a ultrassonografia.
Leia mais sobre histeroscopia diagnóstica no tratamento da infertilidade!
Exames de imagem
Realizada na fase folicular final do ciclo menstrual, favorece a observação da cavidade endometrial e a identificação de pólipos, sinéquias e miomas submucosos, além de verificar a presença ou ausência de folículo dominante nos ovários.
Se houver suspeita de endometriose, a ultrassonografia transvaginal e a ressonância magnética da pelve, realizadas após preparo intestinal, são métodos com maior sensibilidade para diagnóstico e mapeamento das lesões.
Pesquisa de trombofilias
A pesquisa de trombofilias no contexto da infertilidade é fundamental, pois condições trombofílicas podem interferir na implantação embrionária e aumentar o risco de abortos recorrentes.
Inicialmente, é importante realizar exames para identificar mutações genéticas como o fator V de Leiden e a mutação da protrombina, assim como dosar os níveis de proteínas anticoagulantes naturais, como proteína C e proteína S.
Além disso, a detecção de anticorpos antifosfolipídios, incluindo anticoagulante lúpico e anticorpos anticardiolipina, é essencial para avaliar a presença de síndrome antifosfolipídica, que está fortemente associada à infertilidade e perdas gestacionais.
Dessa forma, a identificação precoce e o tratamento adequado das trombofilias podem melhorar significativamente as taxas de sucesso reprodutivo e reduzir os riscos de complicações durante a gravidez, proporcionando um manejo mais seguro e eficaz para as pacientes.
Diagnóstico de infertilidade masculina
A primeira etapa no diagnóstico da infertilidade masculina é a coleta de uma história clínica completa. Essa história deve incluir detalhes sobre a história sexual e reprodutiva, como a:
- Frequência e a regularidade das relações sexuais
- Tentativas anteriores de concepção
- Histórico de doenças sexualmente transmissíveis.
A história médica e cirúrgica do paciente também é essencial, abrangendo doenças crônicas, cirurgias abdominais ou pélvicas, traumas testiculares e uso de medicamentos. Além disso, é importante considerar a história ocupacional e de estilo de vida, com foco na exposição a toxinas, radiações, calor excessivo e o consumo de álcool, tabaco e drogas recreativas.
O exame geral deve avaliar sinais de hipogonadismo, como a distribuição de pelos bem como o desenvolvimento muscular. Já o exame genital envolve a inspeção dos testículos, epidídimos, ductos deferentes e pênis, buscando identificar anormalidades como varicocele, hidrocele, criptorquidia ou ausência dos ductos deferentes.
Exames laboratoriais e de imagem
A análise seminal é fundamental no diagnóstico da infertilidade masculina, avaliando parâmetros como:
- Volume
- pH
- Concentração de espermatozoides
- Motilidade
- Morfologia e presença de leucócitos.
Deve-se analisar após um período de abstinência sexual de 2 a 7 dias. Contudo, testes adicionais podem incluir a fragmentação de DNA espermático, teste de vitalidade e avaliação da capacidade de penetração no muco cervical.
Além disso, a avaliação hormonal também é essencial e inclui a dosagem de hormônios sexuais como testosterona total e livre, hormônio folículo-estimulante (FSH), hormônio luteinizante (LH) e prolactina. A avaliação da função tireoidiana, através da dosagem de TSH e T4 livre, pode ser necessária em pacientes com suspeita de disfunção tireoidiana.
Dessa forma, realiza-se exames genéticos, como cariótipo e pesquisa de microdeleções na região AZF do cromossomo Y, para identificar anomalias cromossômicas. O teste de fibrose cística é indicado em casos de ausência bilateral dos ductos deferentes.
A ultrassonografia escrotal é útil para avaliar varicocele, tumores testiculares e outras anomalias estruturais, enquanto a ultrassonografia transretal é indicada para detectar obstruções nos ductos ejaculatórios e anomalias da próstata e vesículas seminais.
Testes de função espermática
Realiza-se testes de função espermática, como o teste de capacidade de reação acrossômica bem como o teste de ligação de espermatozoides ao muco cervical, para avaliar a capacidade dos espermatozoides de reagirem e penetrarem o óvulo, e sua capacidade de penetração e migração através do muco cervical, respectivamente.
Abordagem no tratamento da infertilidade sem causa aparente
No manejo da infertilidade inexplicada, é essencial equilibrar a eficácia, os custos, a segurança e os riscos das opções terapêuticas disponíveis.
Uma estratégia comum consiste em começar com tratamentos que demandem menos recursos, conduzidos pelo paciente, como mudanças no estilo de vida ou relações programadas. Em seguida, avança-se gradualmente para opções mais intensivas, como o uso de citrato de clomifeno (CC) combinado com inseminação intrauterina (IIU), e, por fim, para intervenções de alto custo, como injeções de gonadotrofinas associadas à IIU e fertilização in vitro (FIV).
Deve-se ocorrer uma abordagem terapêutica personalizada para atender às necessidades individuais de cada casal. Assim, caso um tratamento específico de fertilidade não resulte em gravidez após três ciclos, recomenda-se considerar outras alternativas.
Citrato de clomifeno (CC) combinado com inseminação intrauterina (IIU)
Assim, após a abordagem de questões relacionadas ao estilo de vida, o tratamento é iniciado com CC/IIU ou letrozol/IIU. Portanto, como as mulheres com infertilidade inexplicada geralmente ovulam normalmente, o objetivo da indução da ovulação é estimular suavemente os ovários para alcançar a dupla ovulação em mulheres que normalmente ovulam apenas uma vez.
Assim, a combinação de CC com IIU baseia-se na hipótese de que a colocação de um grande número de espermatozoides nas partes superiores do trato reprodutivo aumenta as chances de concepção.
Fertilização in vitro (FIV)
Para mulheres que não concebem após três a quatro ciclos de tratamento com CC ou letrozol/IIU, o próximo passo é a FIV. Reconhece-se a FIV por apresentar as maiores taxas de sucesso por ciclo em um intervalo de tempo mais curto, com até 40% dos ciclos resultando em nascimento vivo, no entanto, é também a opção de tratamento mais dispendiosa.
Para mulheres que não podem optar pela FIV devido a razões financeiras, de seguro, religiosas ou pessoais, são oferecidas opções como indução da ovulação com gonadotrofinas injetáveis ou laparoscopia. Além disso, para mulheres assintomáticas, recomenda-se a indução da ovulação com outro agente oral ou com gonadotrofinas e IIU, pois esta última apresenta taxas mais elevadas de concepção em comparação com CC/IIU ou inibidores da aromatase.
No entanto, é importante informar às pacientes que a gonadotrofina/IIU também está associada a um aumento na taxa de gestações múltiplas, incluindo trigêmeos e gestações de ordem superior, em comparação com CC ou letrozol.
Conheça nossa pós em Sexualidade Humana
Você está pronto para expandir seus horizontes e transformar sua carreira? Nossa pós-graduação em Sexualidade Humana é a oportunidade perfeita para você!
Referências
- American Society for Reproductive Medicine. Five things physicians and patients should question. Philadelphia: ABIM Foundation. 2013. Disponível aqui. Acesso em 29 de Junho de 2024.
- Gibbons et. al. Unexplained infertility. 2022. UpToDate. Disponível aqui. Acesso em 29 de Junho de 2024.
- Esteves SC, Miyaoka R, Agarwal A. An update on the clinical assessment of the infertile male. [corrected]. Clinics (Sao Paulo). 2011;66(4):691-700.
- World Health Organization. WHO laboratory manual for the examination and processing of human semen, 5a ed. Geneva: World Health Organization; 2010.